“La regla final de los Programas de Verificación de Proveedores Extranjeros (FSVP), establecida a través de la Ley de Modernización de Seguridad Alimentaria de la FDA (FSMA), requiere que los importadores verifiquen que los alimentos que están importando a los Estados Unidos se hayan producido de una manera que cumpla con los estándares de inocuidad alimentaria aplicables.
7 de octubre de 2019.-
Para hacer esto, los importadores deben desarrollar, implementar y mantener un Programa de verificación de proveedores extranjeros que incluya actividades de verificación y registros de esas actividades para cada alimento importado de cada proveedor extranjero. Durante una inspección FSVP, el investigador de la FDA revisará los registros del importador para determinar su cumplimiento con la regulación FSVP. Para ayudar a los importadores a determinar los registros FSVP que deben desarrollar y mantener, la FDA ha puesto a disposición una lista de registros requeridos por la regulación FSVP.”
Introducción
Hemos reelaborado el documento con el objetivo de acercar a las empresas EXPORTADORAS de alimentos a USA, un resumen de los requisitos que le solicitará su contraparte importadora.
Si se trata de productos de baja acidez enlatados o materias primas e ingredientes que se utilizarán para elaborar este tipo de productos, el FSVP abordará los siguientes registros básicos comunes a todos los productos:
Respecto de las BUENAS PRÁCTICAS DE MANUFACTURA:
Además de los requisitos conocidos de siempre – TITLE 21–FOOD AND DRUGS, CHAPTER I–FOOD AND DRUG ADMINISTRATION, DEPARTMENT OF HEALTH AND HUMAN SERVICES, SUBCHAPTER B–FOOD FOR HUMAN CONSUMPTION, PART 110 CURRENT GOOD MANUFACTURING PRACTICE IN MANUFACTURING, PACKING, OR HOLDING HUMAN FOOD – se requerirá que la gerencia se asegure de que todos los empleados que fabrican, procesan, empaquetan o retienen alimentos estén calificados para realizar sus tareas asignadas.

https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=110
Dichos empleados deberán tener la combinación necesaria de educación, capacitación y / o experiencia necesaria para fabricar, procesar, empacar o mantener alimentos limpios e inocuos. Las personas deberán recibir capacitación en los principios de higiene e inocuidad de los alimentos, incluida la importancia de la salud e higiene de los empleados según corresponda al alimento, la instalación y las tareas asignadas de la persona.
Dichos empleados deberán tener la combinación necesaria de educación, capacitación y / o experiencia necesaria para fabricar, procesar, empacar o mantener alimentos limpios e inocuos. Las personas deberán recibir capacitación en los principios de higiene e inocuidad de los alimentos, incluida la importancia de la salud e higiene de los empleados según corresponda al alimento, la instalación y las tareas asignadas de la persona.
Respecto del PLAN DE INOCUIDAD ALIMENTARIA:
Se requerirá que las instalaciones tengan e implementen un plan de inocuidad alimentaria por escrito que incluya:
Análisis de peligros: el primer paso es la identificación de peligros, que debe considerar los peligros biológicos, químicos y físicos conocidos o razonablemente previsibles. Estos peligros podrían estar presentes porque ocurren de forma natural, se introducen involuntariamente o se introducen intencionalmente para obtener beneficios.
Si el análisis de peligros revela uno o más peligros que requieren un control preventivo, la instalación debe tener e implementar controles preventivos escritos para los peligros identificados.
Controles preventivos: las instalaciones tienen la flexibilidad de adaptar los controles preventivos para abordar los riesgos que ocurren en los productos que fabrican. Los controles preventivos, que deben escribirse, deben implementarse para garantizar que cualquier peligro que requiera un control preventivo se minimice o prevenga significativamente y ayudarán a garantizar que los alimentos no sean adulterados. La regla incluye los siguientes controles preventivos:
Los controles de proceso incluyen procedimientos que garantizan que se cumplan los parámetros de control. Los controles de proceso pueden incluir operaciones tales como cocinar, refrigerar y acidificar alimentos. Deben incluir parámetros y valores (por ejemplo, límites críticos), según corresponda a la naturaleza del control aplicable y su función en el sistema de inocuidad alimentaria de la instalación.
Los controles de alérgenos alimentarios son procedimientos escritos que la instalación debe tener e implementar para controlar el contacto cruzado de alérgenos y garantizar que los alérgenos se enumeren adecuadamente en las etiquetas de los productos alimenticios envasados.
Los controles de saneamiento son procedimientos, prácticas y procesos para garantizar que la instalación se mantenga en condiciones sanitarias para minimizar o prevenir riesgos tales como agentes patógenos ambientales, riesgos de los empleados que manipulan alimentos y riesgos de alérgenos alimentarios.
Otros controles son controles que no se describen anteriormente, pero son necesarios para garantizar que un peligro que requiera un control preventivo se minimice o prevenga significativamente.
Supervisión y gestión de los controles preventivos: una vez que una instalación ha identificado un control preventivo para un peligro, la instalación debe asegurarse de que se cumplan los controles.
Monitoreo: estos procedimientos están diseñados para garantizar que los controles preventivos se realicen de manera consistente. El monitoreo se realiza según sea apropiado para el control preventivo. Por ejemplo, el monitoreo de un proceso de calor para matar patógenos incluiría registrar valores de temperatura. El monitoreo debe estar documentado.
Correcciones: son pasos tomados, de manera oportuna, para identificar y corregir un problema menor y aislado que ocurre durante la producción de alimentos.
Acciones correctivas: éstas incluyen acciones para identificar y corregir un problema implementando un control preventivo, reducir la probabilidad de que el problema vuelva a ocurrir, evaluar la inocuidad de los alimentos afectados y evitar que esos alimentos ingresen al comercio si no puede asegurarse de que los alimentos afectados no estén adulterados. Las acciones correctivas deben documentarse con registros.
Verificación: estas actividades son necesarias para garantizar que los controles preventivos se implementen de manera consistente y sean efectivos para minimizar los riesgos. Los ejemplos de actividades de verificación incluyen la validación científica de los controles preventivos del proceso para garantizar que la medida de control sea capaz de controlar efectivamente un peligro identificado y calibrar (o verificar la precisión de) los instrumentos de monitoreo y verificación del proceso, como los termómetros. Las actividades de verificación también incluyen la revisión de registros para asegurar que se estén llevando a cabo acciones de monitoreo y correctivas (si es necesario). Las actividades de verificación deben estar documentadas.
Las pruebas de productos y el monitoreo ambiental también son posibles actividades de verificación, requeridas según sea apropiado para el alimento, la instalación, la naturaleza del control preventivo y el papel de ese control en el sistema de inocuidad alimentaria de la instalación. Se requiere monitoreo ambiental si la contaminación de un alimento listo para comer con un patógeno ambiental es un peligro identificado que requiere un control preventivo.
Programa de cadena de suministro: los fabricantes importadores deben tener e implementar un programa de cadena de suministro basado en el riesgo si el análisis de peligros identifica un peligro que (1) requiere un control preventivo y (2) el control se aplicará en la cadena de suministro de la instalación.
Las instalaciones importadoras no necesitan tener un programa de cadena de suministro si controlan el peligro en su propia instalación, o si una entidad posterior (como otro procesador) controlará el peligro, y la instalación sigue los requisitos aplicables.
Los fabricantes importadores son responsables de garantizar que las materias primas y otros ingredientes que requieren un control aplicado en la cadena de suministro se reciban sólo de proveedores aprobados, o de manera temporal de proveedores no aprobados cuyos materiales están sujetos a actividades de verificación antes de ser aceptados para su uso. (Los proveedores son aprobados por la instalación después de que la instalación considere varios factores, como un análisis de peligros de los alimentos, la entidad que controlará ese peligro y el desempeño del proveedor).
Otra entidad en la cadena de suministro, como un distribuidor, puede realizar actividades de verificación de proveedores, pero la instalación receptora debe revisar y evaluar la documentación de esa entidad de que verificaron el control del peligro por parte del proveedor.
Plan de retiro del mercado: si el análisis de riesgos identifica un peligro que requiere un control preventivo, la instalación debe tener un plan de retiro del mercado por escrito que describa los procedimientos para realizar el retiro del producto. El plan de retiro del mercado debe incluir procedimientos para notificar a los destinatarios, para notificar al público cuando sea necesario, para realizar controles de efectividad y para eliminar adecuadamente el producto retirado.
Para el resto de los productos, los exportadores pueden ser incluidos en un FSVP o en el programa en cadena de los controles preventivos de alimentos, en cuyo caso los registros son los que se prevén en 21 CFR 117 subparte G.475 sobre Registros que documentan el programa de la cadena de suministro (https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=117&showFR=1&subpartNode=21:2.0.1.1.16.7).
Podrán solicitarse registros de:
(1) Auditorías in situ;
- (i) El nombre del proveedor sujeto a la auditoría in situ;
- (ii) Documentación de los procedimientos de auditoría;
- (iii) Las fechas en que se realizó la auditoría;
- (iv) Las conclusiones de la auditoría;
- (v) Acciones correctivas tomadas en respuesta a deficiencias significativas identificadas durante la auditoría; y
- (vi) Documentación de que la auditoría fue realizada por un auditor calificado;
(2) Muestreo y prueba de la materia prima u otro ingrediente;
- (i) Identificación de la materia prima u otro ingrediente analizado (incluido el número de lote, según corresponda) y el número de muestras analizadas;
- (ii) Identificación de las pruebas realizadas, incluidos los métodos analíticos utilizados;
- (iii) La (s) fecha (s) en que se realizaron la (s) prueba (s) y la fecha del informe;
- (iv) Los resultados de la prueba;
- (v) Acciones correctivas tomadas en respuesta a la detección de peligros; y
- (vi) Información que identifica al laboratorio que realiza la prueba;
(3) Revisión de los registros relevantes de inocuidad alimentaria del proveedor. Por ejemplo:
- (i) El nombre del proveedor cuyos registros fueron revisados;
- (ii) La (s) fecha (s) de revisión;
- (iii) La naturaleza general de los registros revisados;
- El análisis de peligros de los alimentos.
- Los procedimientos, procesos y prácticas del proveedor relacionados con la inocuidad de la materia prima y otros ingredientes.
- Regulaciones aplicables de inocuidad alimentaria de la FDA e información relevante para el cumplimiento del proveedor con esas regulaciones
- (iv) Las conclusiones de la revisión; y
- (v) Acciones correctivas tomadas en respuesta a deficiencias significativas identificadas durante la revisión.
En cualquier caso, podrán solicitar información sobre el historial de inocuidad alimentaria del proveedor.
Todas estas evaluaciones deben ser realizadas por un agente independiente del exportador y calificado específicamente para la tarea.
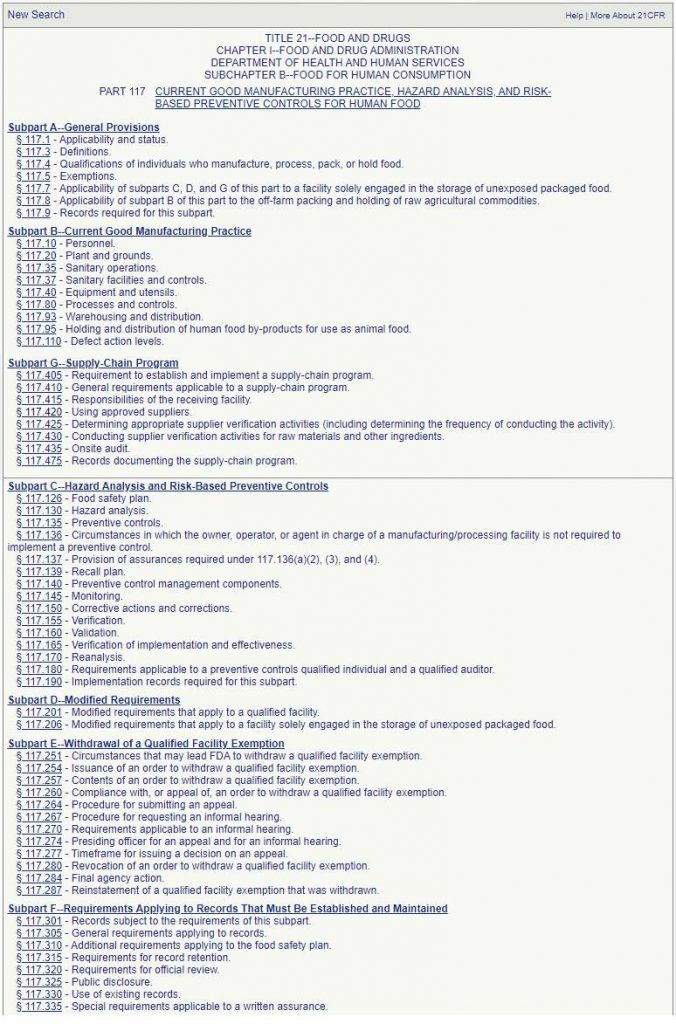
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=117
Registros
Los registros podrán ser guardados como registros originales, copias verdaderas (como fotocopias, fotos, escaneadas copias, microfilm, microfichas u otras reproducciones precisas de los registros originales), o registros electrónicos.
Deberán ser:
Registros firmados y fechados a la finalización inicial y cualquier modificación.
Registros legibles y almacenados para evitar el deterioro o la pérdida.
Registros disponibles de inmediato para el representante autorizado de la FDA, previa solicitud, para inspección y copia.
Traducción al inglés proporcionada dentro de un tiempo razonable, a pedido de la FDA.
Registros almacenados fuera del sitio recuperados y proporcionados en el sitio dentro de las 24 horas posteriores a la solicitud de la FDA.
Registros enviados a la Agencia electrónicamente, o por otro medio de entrega inmediata, previa solicitud escrita de la FDA.
Registros retenidos hasta al menos 2 años después de creado u obtenido, o registros relacionados con procesos y procedimientos retenidos durante al menos 2 años después de que se descontinuó su uso.
Para el caso de importadores muy pequeños la solicitud de una carta de garantía por parte de los exportadores puede ser suficiente. La carta deberá expresar por escrito que se están produciendo alimentos de conformidad con los procesos y procedimientos que brindan protección de salud pública aplicable, antes de importar alimentos y al menos cada 2 años a partir de entonces.
Si así no fuera, habrá que presentar las Acciones correctivas tomadas. Y si correspondiera, los auditores intervinientes deben ser calificados como tales.
Elaboradores de alimentos de países con sistema de inocuidad alimentaria oficialmente reconocido o equivalente.
En estos casos la documentación requerida antes de efectuar la exportación de un alimento y anualmente a partir de entonces será:
> Registro de que se está bajo la supervisión oficial así como los productos dentro del alcance del reconocimiento oficial o determinación de equivalencia.
> Registro de cumplimiento con los requisitos de alimentos comparables o equivalentes.
> Cualquier acción correctiva tomada (si corresponde).
Conclusión
Y aquí termina el relevamiento de registros. Nuestra conclusión es que más allá de los requisitos formales que puedan presentarse, si trabajamos bajo el compromiso de asegurar la inocuidad de nuestros alimentos producidos podemos adaptarnos a las demandas de cualquier mercado.
Se avecinan desafíos y nuevos obstáculos, pero si fijamos el objetivo en la inocuidad tendremos un gran avance y la facilidad de hablar un idioma de comprensión universal.
Autora del artículo:

Paula Feldman.
Ingeniera Agrónoma y Especialista en Agronegocios y Alimentos (UBA).
Es directora de Portal de Inocuidad desde el año 2012. Ha dirigido Axonas desde el año 2000, durante 18 años. Es docente en diversos ámbitos profesionales y actúa como experta técnica en actividades de acreditación de organismos de certificación.
Fue responsable de las actividades de capacitación del Programa Calidad de los Alimentos Argentinos, entre 1997 y el 2005.
Ha escrito numerosas publicaciones sobre calidad en alimentos y cuenta con formación de nivel internacional: auditora lider IRCA 9001:2000 y 22000, auditora BRC, capacitadora en calidad e inocuidad de los alimentos de INPPAZ.
Ha diseñado y dictado 50 cursos abiertos en los últimos 4 años sobre Prerrequisitos del HACCP, HACCP avanzado y temas de actualización, Documentación de sistemas de gestión de calidad de alimentos, Trazabilidad, Resolución de No conformidades, Implementación de normas.
Cursos dictados por la docente:
Ver calendario.
Portal de Inocuidad © Se prohíbe la reproducción total o parcial de los contenidos sin citar su fuente o solicitar autorización.


Aquí pueden dejarnos sus comentarios