Con las herramientas y técnicas apropiadas se puede confirmar, con un alto grado de confianza estadística, la efectividad de una medida de control para reducir un peligro específico a un nivel o concentración aceptable que sea consistente con valor aceptable del peligro en el producto final.
El concepto de medida de control no es nueva, lo que es nuevo, es que la BRCGS, en su V9, y para alinearse con el Codex del 2020, especifica en el requisito 2.7.4; que “Cuando el control de un peligro de seguridad alimentaria determinado se logre mediante programas de prerrequisitos o medidas de control distintas de los CCP; esto se deberá declarar y se deberá validar la idoneidad del programa para controlar dicho peligro “.
La definición del Codex de validación es “La obtención de pruebas que demuestren que una medida de control o combinación de medidas de control, si se aplica debidamente, es capaz de controlar el peligro con un resultado especificado”.
La nueva definición de validación de FSMA establece algo diferente: «Validación significa obtener y evaluar evidencia científica y técnica de que una medida de control, una combinación de medidas de control o el plan de inocuidad de los alimentos en su conjunto, cuando se implementa adecuadamente, es capaz de controlar de manera efectiva los peligros identificados«. Y aquí entramos con esta idea de las herramientas que nos brinda la estadística en el proceso de validación. El principio fundamental que respalda la validación es el requisito de probar un proceso o procedimiento capaz de cumplir con un resultado especificado predeterminado con un alto grado de certeza estadística y reproducibilidad.
Por lo tanto, la efectividad de la medida de control debe validarse para confirmar su capacidad y confiabilidad con respecto al peligro identificado. Sin estas guías, es imposible verificar la capacidad o el rendimiento de un proceso en la medida necesaria para garantizar la inocuidad de los alimentos.
¿Lo vemos con un ejemplo?
Si tenemos un equipo compartido para la elaboración un producto para consumidor final que difiere en un alérgeno (SO2) en su etiquetado, y la empresa ha identificado la limpieza de ese equipo como una media de control para eliminar el peligro a un nivel razonable (< 10 ppm) tal que NO se declara en la etiqueta con la advertencia precautoria de “puede contener”; estamos en un caso para explicar este modelo de validación de medida de control más allá de un PCC.
El muestreo debería basarse en el uso de técnicas de muestreo, planes de muestreo y metodologías de ensayo adecuadas. Los datos recogidos deberían ser suficientes para los análisis estadísticos requeridos. Por ello, podemos hacer un estudio de la capacidad del proceso, Cp. Es decir, evaluar si el proceso es potencialmente capaz de cumplir con la especificación planteada (<10 ppm luego de la limpieza).
No necesitamos necesariamente un valor alto de Cpk, ya que no necesitamos una indicación de que el proceso está centrado entre los límites de las especificaciones, ya que no hay lógica basada en inocuidad de alimentos para tener un límite inferior. Podemos demostrar que, analizando SO2 luego de la limpieza en el equipo compartido, para este producto, con el protocolo de limpieza establecido, en al menos 30 puntos de muestreo durante un período de tiempo no menos a 3 semanas, bajo el escenario más desfavorable; los valores de SO2 son menores a 10 ppm, con un Cp de 1.91, como muestra el gráfico:
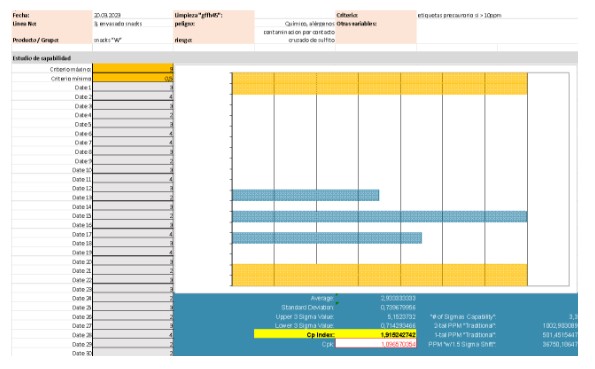
Y validamos de esta manera nuestra medida de control.
Referencias:
- Food Safety Objectives: The Nexus among Preventive Controls, Validation, and Food Safety Assurance, 02/2023, Food Safety Magazine.
- Guidance for Industry Process Validation: General Principles and Practices; 01/2011, FDA.
- CAC/GL 69-2008: Directrices para la Validación de Medidas de Control de la Inocuidad de los Alimentos.
- Guía Simplificada para el Entendimiento y Uso de Objetivos de Inocuidad de los Alimentos y Objetivos de Rendimiento; ICMSF, 2006.
Autora

Leila Burin.
Coordinadora Académica de Portal de Inocuidad.
PhD en Ciencias Químicas, Universidad de Buenos Aires, 2001 y Lic. en Ciencias Biológicas, Universidad de Buenos Aires.
2010 hasta la fecha: auditora GFSI: Esquemas: IFS, BRCGS, ISO 22 000, FSSC 22000, y esquemas privados, como SQMS (Mac Donalds) con base en España.
1997 hasta la fecha: QualyFoods S.A. como Directora. Digitalización de procesos: Q-Chess mobile y asesoramiento en inocuidad alimentaria. Capacitadora reconocida: HACCP Alliance Lead Instructor y BRCGS ATP (2019/2022).
2022 hasta la fecha: representante ENFIT en España.
Portal de Inocuidad © Se prohíbe la reproducción total o parcial de los contenidos sin citar su fuente o solicitar autorización.


Buenas noches. Disfruté de este artículo y como siempre uds aportando a la causa. El Cp de 1.91 es casi el doble (casi abarca 2 histogramas) y se considera aceptable después de 1,33. Pregunta,¿existe referencia de valores mínimos de Cp para validación?. Gracias y feliz navidad